作者简介:占升(1992—),男,江西上饶人,硕士研究生,从事土壤修复相关研究。E-mail:dwyanezs3@163.com
分别以过氧化氢、过碳酸钠和过氧化钙活化过硫酸钠降解蒽、芘及苯并芘3种多环芳烃,并对其反应过程进行动力学讨论及降解产物分析。结果表明,3种氧化剂活化过硫酸钠的效果依次为过碳酸钠>过氧化氢>过氧化钙。在温度25 ℃,土与水均为5 g,过碳酸钠与过硫酸钠在水中浓度分别为0.67及1.0 mmol·g-1,反应时间180 min时,蒽、芘和苯并芘的降解率分别为96.8%、93.5%和96.8%。动力学考查结果表明,过碳酸钠和过氧化氢活化过硫酸钠降解多环芳烃的反应符合一级反应动力学规律,且土壤中绝大部分多环芳烃被降解。
Activated sodium persulfate by hydrogen peroxide, sodium percarbonate and calcium peroxide were used to removal anthracene, pyrene, and benzoapyrene (PAHs) in soil, respectively. In addition, the kinetics and by-products in the reaction process of PAHs were investigated. The results showed that the activation effect on sodium persulfate was in the order of sodium percarbonate>hydrogen peroxide>calcium peroxide. The degradation rate of anthracene, pyrene and benzoapyrene was 96.8%, 93.5% and 96.8%, respectively, in the case of sodium persulfate activated by sodium percarbonate with the following condition: reaction time of 180 min, temperature of 25 ℃, soil and water both 5 g, and the concentration of sodium persulfate, sodium percarbonate in water of 1.0 and 0.67 mmol·g-1. Kinetic analysis indicated that degradation of PAHs by sodium persulfate activated by sodium percarbonate and hydrogen peroxide both were complying with first order reaction kinetics, and the vast majority of PAHs in the soil were degraded.
多环芳烃(polycyclic aromatic hydrocarbons, PAHs)是一类具有致癌、致畸、致突变特性, 且难被生物降解的疏水性有机污染物[1], 其在环境中有极强的迁移能力, 与水和大气相比, 富含有机质的土壤更易成为多环芳烃的中转站和仓库[2, 3]。随着全球工业化的发展, 大量的多环芳烃被排放到环境中, 造成土壤中多环芳烃的浓度不断增加[4], 给人类健康和生态环境带来严重的威胁; 因此修复多环芳烃污染土壤已成为环保领域的难点和热点。
土壤中多环芳烃的修复方法主要有物理修复、化学修复和生物修复3大类[5], 其中化学修复中的原位化学氧化技术是目前具有较大发展前景的一种污染土壤修复技术[6], 其主要过程是通过直接向污染土壤中注入氧化剂使污染物降解转化成无害化的物质。过硫酸盐作为原位化学氧化技术中新兴的一种修复剂, 其氧化过程具有稳定性好、pH适用范围广、绿色无毒的特点。其氧化过程的机理是, 在活化方式的作用下致使本身的— O— O— 断裂产生具有强氧化性的S
上述的活化过硫酸盐的技术在各研究方向上都取得了一定的成果, 但各活化方式均因自身缺陷而制约了其在工程化上的应用, 例如, 热活化的能耗较大, 而紫外光活化的实际应用困难; 因此, 开发更高效、绿色的活化方式是目前过硫酸盐领域研究的热点。在本课题组前期的研究中, 考查了不同金属离子活化过硫酸盐降解土壤中芘的效果, 考虑到金属离子的潜在风险, 本研究拟采用环境风险较小的氧化剂作为活化剂, 其与过硫酸盐构成的双氧化剂体系可进一步提高氧化效率。过氧化氢是一种绿色的氧化剂, 过碳酸钠和过氧化钙是以固体为载体的过氧化氢[11, 12, 13], 以不同载体的过氧化氢作为活化剂活化过硫酸盐还未见诸报道, 故本研究以3种代表性多环芳烃— — 蒽、芘和苯并芘为目标污染物, 通过对比研究过碳酸钠、过氧化氢和过氧化钙活化过硫酸钠对其降解的效果, 筛选出活化效果优异的氧化剂, 并进一步探讨活化过硫酸钠降解土壤中多环芳烃的动力学特征及降解产物, 为多环芳烃污染场地修复提供基础依据。
过硫酸钠(Na2S2O8)购自上海申博化工有限公司; 过氧化氢(30%, H2O2)、过氧化钙(70%, CaO2)购自国药集团化学试剂有限公司; 二氯甲烷(CH2Cl2)、正己烷(C6H14)、乙腈(C2H3N)购自江苏强盛功能化学股份有限公司。以上试剂皆为分析纯。过碳酸钠(Na2CO3· 1.5H2O, 优级纯)购自赛默飞世尔科技有限公司; 蒽(Anthracene, C14H10, 纯度99%)、芘(Pyrene, C16H10, 纯度98%)、苯并[a]芘(benzoapyrene, C20H12, 纯度95%)购自北京百灵威科技有限公司。
实验用土壤采自上海化工研究院绿地深层土壤, 土壤样品置于阴凉处自然风干, 研磨过60目筛后储存备用。用激光粒度仪(Mastersizer 2000型, 马尔文仪器有限公司)测得土壤为粉砂壤土, 参考《土壤和固体废物污染物分析测试方法》[14]测得供试土壤理化性质:土壤pH值8.9; 土壤颗粒组成黏粒:粉料:砂粒为2.79%:63.00%:34.21%; 土壤有机质含量7.0 g· kg-1; 土壤中Mn、Cu、Zn含量分别为464.1、23.6、113.9 mg· kg-1, 土壤铁含量为16.9 g· kg-1; 土壤中Cd、Hg、蒽、芘、苯并芘未检出。
称取200 g土壤于500 mL烧杯中, 加入适量溶有0.02 g蒽、0.04 g芘、0.03 g苯并芘的二氯甲烷溶液混合均匀, 将烧杯置于通风橱中待二氯甲烷完全挥发, 老化14 d后测得土壤中蒽、芘、苯并芘的染毒量分别为92.4、199.5、144.9 mg· kg-1。
以土壤中多环芳烃为目标污染物, 分析比较不同氧化剂活化过硫酸钠的活化效果, 设计15个反应, 涉及3种氧化剂, 每种氧化剂5个水平, 且3种氧化剂对应各水平的理论过氧化氢投加量相等, 过碳酸钠和过氧化钙溶于水中理论生成过氧化氢的量分别见式(1)、式(2)。每个反应设有重复实验, 具体如表1所示, 均在25 ℃恒温水浴、水与土各5 g、反应时间120 min的条件下进行。
2(Na2CO3· 1.5H2O2) → 2Na2CO3+3H2O2; (1)
CaO2(s)+2H2O → H2O2+Ca(OH)2(s)。 (2)
其后, 选取活化效果优异的氧化剂开展实验, 分析其活化过硫酸钠降解土壤中多环芳烃的降解动力学过程和降解产物。
| 表1 实验方案设计 Table 1 Experimental design |
具体实验步骤如下:精确称取5.00 g染毒土壤放入150 mL广口瓶中, 按水土体积质量比1:1加去离子水配成泥浆, 分别加1 mmol· g-1(依据土壤质量)的过硫酸钠和一定量的氧化剂, 在25 ℃条件下(恒温水浴)磁悬搅拌一定时间后, 将广口瓶置于冰箱中冷冻15 min以终止反应, 反应后的泥浆经真空抽滤分离, 所得滤土冷冻干燥, 最后对土壤和反应液中残余的多环芳烃进行分析。
1.5.1 土壤中多环芳烃浓度的测定
参考超声提取法[15, 16]萃取土壤中的多环芳烃, 具体实验步骤为:精确称取1.00 g冷却干燥后土壤置于15 mL离心管中, 分别加入5 mL二氯甲烷和正己烷作为提取液, 超声提取30 min后, 离心分离, 所得离心液倒入旋蒸瓶中, 加入提取液重复操作1次。将旋蒸瓶中的离心液在旋转蒸发仪上蒸干, 加入适量乙腈, 在旋转蒸发仪上蒸至1 mL左右的浓缩液, 向浓缩液加乙腈定容至10 mL, 过0.45 μ m滤膜去除颗粒物后, 采用高效液相色谱测定多环芳烃的浓度。土壤中PAHs去除率(R)的定义如下:
R=(C1-C2)/C1× 100%。 (3)
式(3)中:C1为土壤中原始多环芳烃浓度(mg· kg-1), C2为土壤中残余多环芳烃浓度(mg· kg-1)。
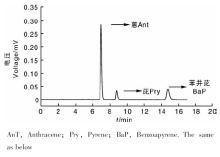
超高效液相色谱检测条件:Athena C18-WP色谱柱, 柱温30 ℃, 流动相为V(乙腈):V(水)=85:15, 流速为0.7 mL· min-1, 紫外检测器, 进样量5 μ L。此时, 3种多环芳烃的图谱如图1所示。
1.5.2 反应液成分分析
反应液中有机成分采用液液萃取法提取, 萃取方法参考HJ 478— 2009, 得到的溶液过0.45 μ m滤膜去除颗粒物后进行GC-MS检测。检测条件:色谱柱为HP-5MS(30 m× 0.25 mm× 0.25 μ m, Agilent, 美国), GC进样口270 ℃, 载气流速1.0 mL· min-1, 分流比5:1。升温程序:初始温度60 ℃保持2 min, 以20 ℃· min-1升至200 ℃不停留, 再以10 ℃· min-1升至270 ℃, 保持4 min。质谱工作模式为全扫描(full scan), 四级杆温度150 ℃, 离子源温度200 ℃, 电子轰击能70 eV。
过氧化氢投加量对过硫酸钠降解多环芳烃的影响如图2所示:过氧化氢和过硫酸钠物质的量之比从0.5:1增加到1:1时, 多环芳烃的降解率逐渐增大, 当其物质的量之比为1:1时, 蒽、芘和苯并芘的降解率最高, 分别达86.4%、66.4%和88.8%; 过氧化氢和过硫酸钠物质的量之比大于1:1时, 降解率呈下降趋势。
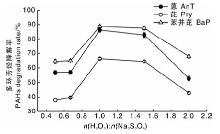 | 图2 不同投加量过氧化氢活化过硫酸钠对多环芳烃降解的影响Fig.2 Effects of activated sodium persulfate by different dosage of hydrogen peroxide on PAHs degradation |
由式(4)、式(5)可知, 过氧化氢活化过硫酸钠的反应中, 若过氧化氢的投加量偏少会导致活化产生的S
H2O2 → H
H
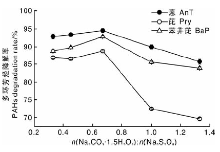
过碳酸钠投加量对过硫酸钠降解多环芳烃的效果如图3所示:当过碳酸钠和过硫酸钠物质的量之比在0.33:1~0.67:1范围内时, 多环芳烃的降解率较高, 当二者物质的量之比为0.67:1时, 蒽、芘、苯并芘的降解率最高, 分别为94.6%、88.8%、92.9%; 但当过碳酸钠和过硫酸钠物质的量之比进一步增大时, 多环芳烃的降解率呈下降趋势。结果表明, 少量的过碳酸钠的投加即可对过硫酸钠产生优异的活化效果, 主要原因可能是过碳酸钠溶于水可以缓慢产生过氧化氢[18], 从而可以更有效地活化过硫酸钠产生S
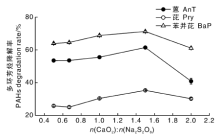
过氧化钙投加量对过硫酸钠降解多环芳烃的效果普遍不佳, 如图4所示, 蒽、芘、苯并芘的降解率达到最大时也仅为61.5%、35.3%、71.3%。当过氧化钙和过硫酸钠物质的量之比大于1.5:1时, 多环芳烃降解率呈下降趋势。Northup等[13]在将过氧化钙用于替代芬顿体系中过氧化氢时发现, 过氧化钙生成过氧化氢的量受pH值的影响, 在pH> 7的条件下过氧化钙很难产生过氧化氢。本研究中泥浆的检测pH=8.9> 7, 因此在实际反应过程中, 过氧化钙仅产生了极少量的过氧化氢, 影响了S
修复技术开发的最终目标是工程化应用, 因此修复技术的经济性是一项重要的评价指标。由2.3节结果可知, 过氧化钙活化过硫酸钠对多环芳烃降解率较低, 故本部分主要对比过氧化氢和过碳酸钠的经济性。以苯并芘降解率88.8%为考查指标, 由图2和图3可知, 除了共同所需的5.0 g水和1.19 g过硫酸钠外, 过氧化氢和过碳酸钠的投加量分别为0.57和0.26 g。工业用过硫酸钠、过氧化氢、过碳酸钠和水的价格分别为5元· kg-1、2元· kg-1、18元· kg-1和4.1元· t-1。以1 t污染土壤为例, 处理所需费用如图5所示, 可以看出, 过氧化氢活化过硫酸钠体系的经济性优于过碳酸钠; 但综合运输、储存以及安全性的因素, 以固体形式存在的过碳酸钠较过氧化氢更有优势, 更有利于工程化应用。
为了进一步了解土壤中多环芳烃在不同氧化剂活化过硫酸钠体系下的降解过程和反应特征, 根据2.1节和2.2节的实验结果, 分别考查最佳投加量的过碳酸钠(0.67 mmol· g-1)和过氧化氢(1 mmol· g-1)活化过硫酸钠降解土壤中多环芳烃的降解动力学过程。反应温度为25 ℃, 水与土均为5 g, 取样时间点分别为10、30、60、120、180 min。
首先, 假设2种氧化体系对多环芳烃的降解反应均符合一级反应动力学方程:Ct =C0 exp(-kt)。
其中:Ct和C0分别为t时刻、0时刻多环芳烃的浓度(mg· kg-1), k为反应速率常数(min-1)。以t为横坐标, ln(Ct/C0)为纵坐标, 分别对两者的实验结果进行拟合, 结果如表2和图6、图7所示。
| 表2 多环芳烃降解的动力学特征 Table 2 Kinetics of PAHs degradation |
由表2和图6可知, 过碳酸钠活化过硫酸钠对3种多环芳烃的降解动力学过程均符合一级反应动力学方程, 模拟结果的线性相关性良好, R2(相关系数)均大于0.96, 蒽、芘、苯并芘的反应速率常数分别为0.018、0.016、0.017 min-1, 芘的降解速率稍慢于蒽和苯并芘。
由表2和图7可知, 过氧化氢活化过硫酸钠对3种多环芳烃的降解动力学过程也均符合一级反应动力学方程, 模拟结果的线性相关性良好, R2(相关系数)均大于0.95, 蒽、芘、苯并芘的反应速率常数分别为0.015、0.011、0.019 min-1, 苯并芘的降解速率最快。
以上结果表明, 在过碳酸钠和过氧化氢活化过硫酸钠的氧化体系下, 芘的降解率较低, 而蒽和苯并芘的降解率相对较高。此结果与赵丹等[9]在开展活化过硫酸钠对污染场地多环芳烃修复的研究中得出的结论相符, 该研究中蒽和苯并芘的降解率在95%以上, 而芘的降解率仅为80%。可能的原因是, 相较于奇数环的多环芳烃, 偶数环的多环芳烃的结构更为紧密、整齐, 从而更难以被S
为考查本研究方法下多环芳烃降解产物对环境的影响, 在过碳酸钠活化过硫酸钠的氧化体系下, 分别对染毒土壤及未染毒土壤(背景土)进行氧化反应, 对其反应液进行液液萃取, 萃取液经GC-MS分析, 其匹配成分见表3。
| 表3 土壤氧化后反应液组分 Table 3 Components of reaction liquid of oxidized soil |
由表3可知, 未染毒土壤反应液成分以烷类、醚类为主, 而染毒土壤的反应液中检测出有机物2-甲基丙酮和1-甲基萘, 可能是多环芳烃的降解产物。本反应对多环芳烃的平均降解率高达95.7%, 而多环芳烃的生物毒性远大于其降解产物[19], 表明本研究方法可降低原污染土壤的环境风险。
(1)不同氧化剂活化过硫酸钠降解多环芳烃实验表明, 过碳酸钠是最佳活化剂, 在温度25 ℃, 水与土各5 g, 过碳酸钠与过硫酸钠在水中浓度分别为0.67及1.0 mmol· g-1, 反应时间为180 min的条件下, 蒽、芘、苯并芘的降解率分别为96.8%、93.5%、96.8%。
(2)反应动力学考查结果表明, 过碳酸钠和过氧化氢活化过硫酸钠降解土壤中蒽、芘、苯并芘的过程均符合一级反应动力学方程, 蒽和苯并芘的降解速率大于芘。
(3)经济性分析表明, 过氧化氢作为活化剂的经济性优于过碳酸钠。GC-MS分析表明, 多环芳烃污染土壤经活化过硫酸钠处理之后, 其环境风险降低。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|