作者简介:单颖(1988—),浙江绍兴人,博士,主要从事动物病原生物学和免疫学研究。E-mail:shanying@zju.edu.cn
猪代尔塔冠状病毒(porcine deltacoronavirus,PDCoV)是一个新发现的致病性猪肠道冠状病毒,目前在中国部分省份养殖场的腹泻病猪中已检测到,并已证实在中国流行。本研究旨在探明PDCoV在浙江省的流行现状和分子演化特征。结果显示,建立的PDCoV一步法TaqMan探针荧光定量检测方法特异,检测灵敏度可达3.94×102拷贝·μL-1,扩增效率为108%, R2值为0.997,标准曲线方程为 Y=-3.156 X+1.826。2013年4月—2016年12月收集的258份仔猪临床腹泻样本中没有检测到,但在2017年1—4月检测阳性率达到50%(12/24)。获得的7个临床分离株的S基因与参考株相比,其核苷酸和氨基酸的同源性分别为99.98%~100%和99.99%~100%;与最初在香港分离到的毒株和美国流行株相比,存在3个碱基缺失和一定数量的突变。以S蛋白进行分子演化分析,发现7株临床分离株均在代尔塔冠状病毒属进化分支上,且与中国分离到的其他PDCoV毒株在进化关系上较近,与美国、泰国等地分离到的PDCoV在进化关系上较远,提示PDCoV的流行株分布有一定的地域性。研究结果提供了浙江省地区PDCoV临床分离株的基因特性,为防控PDCoV引起的仔猪腹泻、加快流行株疫苗的开发提供了数据。
Porcine deltacoronavirus (PDCoV) is a newly discovered pathogenic porcine coronavirus that has been isolated from diarrheal pigs in farms of some provinces in China, confirming that the disease has been prevalent in our country. This study aims to investigate the prevalence and molecular evolution of PDCoV in Zhejiang Province. The results showed that the established PDCoV one-step TaqMan probe was specific for fluorescence quantitative detection. The detection sensitivity was 3.94 × 102 copies·μL-1. The amplification efficiency was 108% and the R2 value was 0.997, regression equation of standard curve is Y=-3.156 X+1.826. The virus was not detected in clinical diarrhea samples of 258 piglests collected from April, 2013 to December, 2016, but the positive rate was 50% (12/24) in the period from January to April, 2017. The homology of the nucleotide and amino acid of the S gene of the seven clinical isolates was 99.98%-100% and 99.99%-100%, respectively. Compared with the reference strain and the Hongkong and American isolated trains, there were three base deletions and a number of mutations in our clinical isolated strains. S-protein was used for the molecular evolution analysis. Seven strains of clinical isolates were found to be belong to the evolutionary branch of the delta virus, and were closer to the other PDCoV strains isolated from China, while farther to the strains isolated from the United States and Thailand, suggesting that PDCoV epidemic strains have a certain geographical distribution. This study provides the genetic characteristics of PDCoV clinical isolates in Zhejiang Province, and provides data for the prevention and control of PDCoV-induced piglet diarrhea and the development of epidemic strains.
冠状病毒属(CoVs)属于冠状病毒科(Coronaviridae), 冠状病毒亚科(Coronavirinae), 冠状病毒亚科中已经描述了4个属, 其中包括:阿尔法冠状病毒(Alphacoronavirus)、贝塔冠状病毒(Betacoronavirus)、伽马冠状病毒(Gammacoronavirus)和代尔塔冠状病毒(Deltacoronavirus)。目前已发现的猪冠状病毒有5种:猪血红蛋白脑炎病毒(PHEV)、猪呼吸道冠状病毒(PRCV)、传染性肠胃炎病毒(TGEV)、猪流行性腹泻病毒(PEDV)和猪代尔塔冠状病毒(PDCoV)。后三者常引起猪肠道疾病, 导致呕吐、腹泻、脱水, 发病率及死亡率较高。其中, PDCoV属于代尔塔冠状病毒属, 2009年在香港的病猪临床样本中首次分离得到[1]。2014年美国报道有PDCoV病情流行, 并迅速蔓延至美国多个州[2, 3, 4, 5, 6]。随后, 韩国、中国、泰国等许多国家也相继发现了PDCoV[7, 8, 9, 10, 11]。据报道, PDCoV与天然感染的临床病例相关, 这些病例主要表现为仔猪严重腹泻, 呕吐和脱水, 以及典型的萎缩性肠炎的组织病理学损伤[12], 发病率和死亡率高达50%~100%[13], 给养猪业造成严重的经济损失。
PDCoV为有囊膜、不分节段的单股正链RNA病毒, 其基因组全长约25 kb, 包括5'端非编码区, 3'端非编码区以及至少7个开放阅读框。其中开放阅读框编码主要的病毒蛋白, 包括ORF1a/1b, 纤突(spike, S)蛋白、小膜(envelope, E)蛋白、膜(membrane, M)蛋白、非结构蛋白6(NS6), 核衣壳(nucleocapsid, N)蛋白, 非结构蛋白7(NS7)[14]。PDCoV诊断方法可分为两类:血清学和病毒学方法[14]。血清学检测可用于确定先前暴露于病毒, 确定抗体对病毒感染的反应动力学, 以及评估疫苗的功效。最常用的血清学测定法包括间接荧光抗体(IFA)测定, 病毒中和(VN)测试或荧光聚焦中和(FFN)测试, 酶联免疫吸附测定(ELISA)和荧光微球免疫测定(FMIA), 但这些测定对PDCoV抗体的检测尚未得到很好的验证[14]。病毒学方法包括病毒颗粒检测(电子显微镜)、病毒核酸检测(RT-PCR和原位杂交)、病毒抗原检测(免疫荧光染色和免疫组织化学)和活病毒检测(病毒分离和猪生物测定)[14]。其中RT-PCR方法能够快速、有效地检测出较低量的病原, 常用于临床检测。因此, 针对病毒特异基因建立RT-PCR检测方法具有较高的应用价值和实际意义。
S蛋白是冠状病毒的重要表面糖蛋白, 并在病毒和细胞表面受体结合以及与细胞膜融合中起重要作用[15, 16]。与其他冠状病毒属成员的S蛋白结构相似, PDCoV的S蛋白有两个功能结构域:N端共价结合域和C端膜锚定的结构域。S蛋白可以类似地分为S1(1~573 aa)和S2(574~1161 aa)两个亚基[17]。S1为主要的病毒抗原, 对被感染宿主中和抗体的产生具有重要的生物学意义。由于受到宿主免疫选择的压力, S蛋白易发生变异, 因此, S蛋白对于了解PDCoV的流行现状、分子多样性、基因突变的联系以及疫苗的发展也有很重要的作用。为了解浙江省周边PDCoV流行情况及流行毒株的分子演化特征, 研究采集杭州市及周边24个地区仔猪腹泻样品, 建立一步TaqMan探针荧光定量检测方法, 对临床病例样本进行PDCoV病原检测, 同时对其中7株临床分离PDCoV毒株的S基因进行克隆和分子特征分析。结果丰富了PDCoV分子流行病学资料, 为疫病准确诊断和有效防控提供了基础数据。
在2013年4月— 2017年4月, 研究采集了浙江省内杭州市及周边24个地区的282份病料, 进行了PDCoV的检测。取发病猪小肠组织及粪便样品, 加适量灭菌的10 mmol· L-1的PBS(pH 7.4)并研磨, 置于-80 ℃冰箱反复冻融2次, 4 ℃ 5 000 r· min-1离心10 min, 取上清。将上清用0.45 μ m的滤膜过滤后, 保存于-80 ℃冰箱。
总RNA提取试剂盒购自天根生化科技有限公司; 逆转录试剂盒购自美国Promega公司; pEASYBlunt载体、DNAMarker DL2000、DNAMarker DL5000、RNA酶抑制剂(HPRI)、dNTP、随机引物、PCR Mix等均购自全式金公司; 琼脂糖购自Sigma公司; 质粒抽提试剂盒、胶回收试剂盒购自杭州柏赞生物试剂开发公司。
参考参考PDCoV CH-01毒株(GenBank No.: KX443143)进行引物设计, 利用VectorNTI软件设计病原检测和S基因克隆所用引物(表1), 其中用3个重叠套式PCR扩增S基因全长, 引物均由上海捷瑞基因科技股份有限公司合成。
| 表1 病原检测和序列克隆所用引物 Table 1 Primers for detecting pathogens and cloning in this study |
取-80 ℃保存的病料样本上清液, 按总RNA提取试剂盒(购于北京天根生化科技有限公司)操作说明书提取病毒总RNA, 核酸经NanoDrop 1000检测浓度为1 800~2 500 ng· μ L-1, D260/D280=1.95~2.05, 保存于-80 ℃。
1.5.1 标准质粒构建
针对PDCoV核衣壳蛋白N基因保守区域设计引物, 以病毒cDNA为模板, 扩增特异性片段。PCR反应体系如下:PDCoV-F/R各0.5 μ L, 高保真PCR Mix 15 μ L, cDNA 2 μ L, ddH2O 12 μ L。反应条件为:预变性 94 ℃ 3 min, 1个循环; 变性94 ℃ 30 s, 1个循环; 退火55 ℃ 30 s、延伸68 ℃, 10 s, 30个循环; 再延伸68 ℃ 10 min, 1个循环。PCR产物经琼脂糖凝胶电泳后割胶回收, 获得纯化产物, 并连接至pEASYBlunt载体, 转化入大肠埃希菌, 挑取单菌落筛选阳性克隆, 测序并保存于-80 ℃备用。
1.5.2 标准曲线构建
抽提标准质粒, 并将标准质粒浓度稀释至20 ng· μ L-1, 其拷贝数为2.146× 1011 拷贝· μ L-1, 标准曲线中记为10-1。将稀释后的标准质粒10倍依次倍比稀释, 分别记为10-2至10-9。设ddH2O为阴性对照孔。反应体系为PDCoV-F/R各0.4 μ L, PDCoV-RTP 0.1 μ L, 质粒5 μ L, ddH2O 5.0 μ L。反应条件为:RT 50 ℃ 10 min, 1个循环; 变性95 ℃ 30 s, 1个循环; 扩增95 ℃ 5 s、60 ℃, 40 s, 45个循环; 复性40 ℃, 30 s, 1个循环。标准曲线要求:R2> 0.99, Slope≈ 0.33, 0.85< 扩增效率E< 1.15。
1.5.3 荧光定量检测病原的反应体系和条件
采用一步法TaqMan探针检测PDCoV, 按LightCycler® Multiplex RNA Virus Master(上海罗氏有限公司)说明, 反应体系为PDCoV-F/R各0.4 μ L, PDCoV-RTP 0.1 μ L, RT-Enzyme Solution 0.1 μ L, RNA sample 5 μ L, ddH2O 5.0 μ L。反应条件为:RT 50 ℃ 10 min, 1个循环; 变性95 ℃ 30 s, 1个循环; 扩增95 ℃ 5 s、60 ℃, 40 s, 45个循环; 复性40 ℃, 30 s, 1个循环。Ct值小于30为阳性, 30~35为可疑, 大于35为阴性。根据Ct值代入标准曲线公式计算其病毒拷贝数。
猪代尔塔冠状病毒PDCoV(ZJ17DQ0301, 分离自浙江德清猪场阳性病料)、猪流行性腹泻病毒PEDV(ZJ15XS01, 分离自浙江萧山猪场阳性病料)、猪传染性胃肠炎病毒TGEV(华毒株)、猪瘟病毒CSFV(C株)、猪圆环病毒2型PCV2(SY4, 分离自浙江上虞猪场阳性病料)、猪繁殖与呼吸综合征病毒PRRSV(JK100疫苗株)和猪链球菌2型SS2(05ZYH33, 分离自猪链球菌2型感染患者)被用于荧光定量特异性检测。以上毒株及菌株均由本实验室保存。
取病毒RNA进行反转录, 反转录步骤简述如下:1 μ g 总RNA与1 μ L的随机引物混匀, RNase-free H2O定容至10 μ L, 混匀后适当离心, 置于65 ℃温浴5 min, 立即放入冰浴5 min, 适当离心后, 加入8 μ L 5× RT缓冲液、4 μ L 2.5 mmol· L-1 dNTP、0.5 μ L RNA酶抑制剂、0.5 μ L反转录酶和RNase-free H2O定容至40 μ L, 充分混匀后, 42 ℃作用 1 h, 95 ℃ 灭活10 min, 获得的cDNA -20 ℃保存备用。
使用特异性引物, 以cDNA为模板, 将S基因分成S-A和S-B两段(分别为1 986 bp和20 05 bp), 利用巢式PCR进行扩增。第一轮PCR反应体系为:ddH2O 5 μ L, 高保真PCR Mix 10 μ L, cDNA 3 μ L, PdCV-CS-S-AF/AR或PdCV-CS-S-BF/BR各1 μ L。PCR程序为:预变性 94 ℃ 3 min, 1个循环; 变性94 ℃ 30 s, 1个循环; 退火52 ℃ 30 s、延伸68 ℃, 2 min, 30个循环; 再延伸68 ℃ 10 min, 1个循环。第二轮PCR反应体系为:ddH2O 20 μ L, 高保真PCR Mix 25 μ L, cDNA 3 μ L, ZJPdCV-AF/AR或ZJPdCV-S-BF/BR各1 μ L。PCR程序为:预变性 94 ℃ 3 min, 1个循环; 变性94 ℃ 30 s, 1个循环; 退火54 ℃ 30 s、延伸68 ℃, 2 min, 30个循环; 再延伸68 ℃ 10 min, 1个循环。
将S基因两个分段S-A及S-B的PCR产物进行1%琼脂糖凝胶电泳, 回收获得目的片段, 并分别克隆至pEASYBlunt载体上, 转化入大肠埃希菌DH5α , 进行保存并测序, 用DNAstar SeqMan软件将S-A及S-B测序所获的序列进行拼接, 得到S基因全长序列。
采用DNAStar中MegAlign version 5.0软件以及DNAMAN软件对获得的PDCoV和我国其他地区的分离株、国外分离株等(表2)的S基因进行核苷酸及氨基酸序列同源性分析; 使用MEGA 5.0中的Neighbor-joining方法进行系统发育进化分析。
| 表2 本试验使用的PDCoV流行毒株及其他参考株 Table 2 Isolates and reference strains used in this study of PDCoV outbreak |
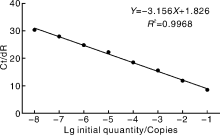
本研究建立的荧光定量PCR方法的检测灵敏度可达3.94× 102拷贝· μ L-1, 且以起始模板浓度的对数值为横坐标, 以各个稀释梯度标准品的RNA含量扩增时达到平台期所需的循环数Ct值为纵坐标时, 在3.94× 108~3.94× 101拷贝· μ L-1呈现良好的直线关系, 且扩增效率为108%, 相关性R2值为0.997(图1)。
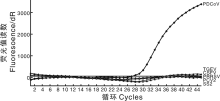
利用本研究建立的荧光定量PCR方法分别检测PDCoV、PEDV、TGEV、猪瘟病毒、猪圆环病毒、猪繁殖与呼吸综合征病毒和猪链球菌等阳性感染样本, 仅PDCoV阳性样本能够得到荧光值读数(图2)。因此, 认为此方法特异性较好, 能够区分不同病原感染样本。
在2013年4月— 2017年4月, 杭州市及周边24个地区采集的282份病料检测结果显示, 2013年4月— 2016年12月收集的258病料中PDCoV的检出率为0, 然而, 2017年1月至4月, 检出率达到50%(12/24)。
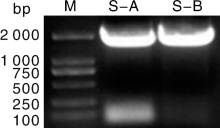
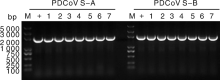
利用特异性引物, 使用巢式PCR方法, 成功克隆S基因2个分段, 如图3所示, PCR产物的电泳结果, 条带清晰, 大小与预期相符。将PCR产物进行回收纯化, 连接至亚克隆载体后转化入大肠埃希菌, 挑取单菌落经PCR鉴定筛选获得阳性克隆(图4), 保存并送测序, 序列拼接后获得S基因全长, 序列上传至NCBI(GenBank Submission ID: 2030821)。由于病料保存问题, 有5份阳性病料抽提所得病毒RNA浓度较低, 因此最终只有7份阳性病料扩增得到全长S基因。
对分离株的S基因序列进行分析发现, 7个毒株S基因全长为3 480 bp, 编码1 160个氨基酸, 与最初在香港分离到的毒株和美国流行的毒株S基因相比有3个碱基缺失, 并存在一定数量的突变。7个毒株的S基因核苷酸同源性及S蛋白氨基酸同源性均较高, 分别为99.98%~100%和99.99%~100%。与其他冠状病毒属成员的S基因核苷酸同源性及S蛋白氨基酸同源性较低(图5)。
以S蛋白进行分子演化分析(图6), 可见SARS-CoV/MERS-CoV/PEDV、Bat Hp-coronavirus/Betacoronavirus HKU24、火鸡冠状病毒(Turkey coronavirus)/鸡传染性支气管炎病毒(IBV)分别位于阿尔法、贝塔、伽马冠状病毒属的进化分支, 而本研究分离所得PDCoV毒株均在代尔塔冠状病毒属进化分支上, 且与中国分离到的其他PDCoV毒株在进化关系上较近, 与美国、泰国等地分离到的PDCoV在进化关系上较远。提示PDCoV的流行株分布有一定的地域性。
2010年12月以来, 中国大陆猪场发生了大量哺乳仔猪腹泻。病原体被认为是猪流行性腹泻病毒(PEDV)的变体, PDCoV在疫情中的作用当时没有进行调查。PDCoV这种新出现的病毒急需有效疫苗的开发, 然而对其流行特征及致病机制的调查和研究非常有限, 需要广泛的监测来界定中国大陆PDCoV的流行病学和进化。
本研究针对PDCoV核衣壳蛋白N基因保守区域设计的特异性TaqMan探针, 建立了一步法荧光定量检测方法。其检测灵敏度可达3.94× 102拷贝· μ L-1, 在3.94× 109~3.94× 101拷贝· μ L-1的监测范围内, 荧光定量Ct值与病毒拷贝数呈现良好的线性关系, 相关性R2值为0.997(图1)。利用本研究建立的荧光定量PCR方法的分别检测PDCoV、PEDV、猪瘟病毒、猪圆环病毒、猪链球菌等阳性感染样本, 仅PDCoV阳性样本能够得到荧光值读数(图2)。因此认为此方法特异性较好, 能够区分不同病原感染样本, 可用于快速诊断PDCoV感染。利用该方法, 既可以检测临床样本PDCoV感染情况, 又可用于检测细胞中病毒增殖情况。
冠状病毒的S蛋白被认为具有较高的遗传变异性, 不仅具有良好的免疫原性, 而且在感染宿主体内介导和抗体产生的过程中起着重要作用[18, 19, 20]。近年来, 由PDCoV引起的猪肠道疾病在生猪主要生产国家受到高度关注, 尤其是美国和中国。已有超过30个完整的PDCoV基因组序列在GenBank数据库中发布[2, 7, 14]。毒株来源除中国和美国外, 分别来自韩国、泰国等地。从利用本研究建立的检测方法检测到PDCoV阳性样本中分离到7株毒株, 利用巢式PCR获得了S基因的截短片段, 通过测序及软件拼接获得了全长, 并对这7个分离株及近年来流行的PDCoV毒株和其他冠状病毒的S基因进行了同源性分析和演化分析。本研究分离所得PDCoV毒株核苷酸及氨基酸的同源性较高, 在进化树上均处于代尔塔冠状病毒属分支上, 且与中国分离到的其他PDCoV毒株在进化关系上较近, 与美国、泰国等地分离到的PDCoV在进化关系上较远, 提示PDCoV的流行株分布有一定的地域性。
本研究建立的一步TaqMan探针荧光定量检测PDCoV方法是一种快速准确的检测方法, 其敏感性高, 特异性好, 可用于快速诊断PDCoV感染。通过对7株PEDV浙江地区毒株及参考株S基因的生物学信息分析表明, 目前在浙江省流行的PEDV毒株与以往国内分离的毒株相比亲缘关系较近, 且存在一定的地域性。本研究为检测临床样本PDCoV感染情况建立了简便、快速、敏感的方法, 为防控PDCoV引起的仔猪腹泻、加快流行株疫苗的开发提供了数据。
(责任编辑 张 韵)
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|